 |
|
Palaute Sivukartta |
|
Etusivu
> Analyysimenetelmät
> 6.2. Potentiometria |
Edellinen | Seuraava | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
6.2. Potentiometria |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
PotentiometriaPotentiometrista mittausta käytetään vetyionien lisäksi myös muiden ionien pitoisuusmäärityksiin. Ioniselektiiviseksi elektrodiksi (ISE, ion selective electrode) valitaan tutkittavalle ionilajille selektiivinen elektrodi, jonka potentiaali määräytyy tämän ionin pitoisuuden mukaan.Mittauksissa tarvitaan ioniselektiivisen elektrodin lisäksi vertailuelektrodi, jonka potentiaali pysyy vakiona ja joka ei häiritse ioniselektiivisen elektrodin toimintaa. Yleensä potentiometrisissa mittauksissa käytetään vertailuelektrodina hopea-hopeakloridivertailuelektrodia. pH-mittauksissa yleensä vertailuelektrodi on rakennettu H+-selektiivisen elektrodin kanssa saman kuoren sisälle, jolloin puhutaan pH-mittauksiin tarkoitetusta yhdistelmäelektrodista. 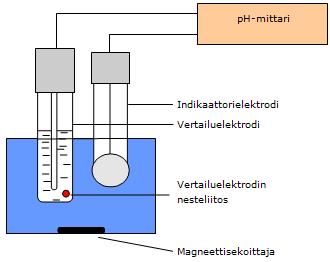 Kuva 1. Potentiometrisen mittauksen periaate Kuvassa 2 on esitetty lasielektrodin rakenne. Taulukossa 1 on esitetty yhteenveto potentiometrisen mittausmenetelmän valinnasta. 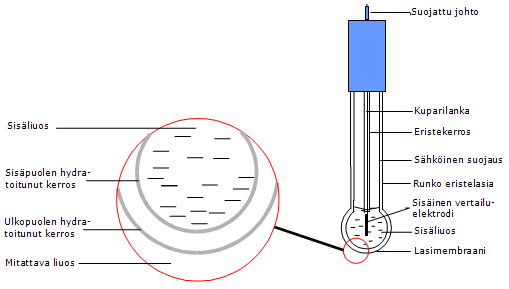 Kuva 2. Lasielektrodin rakenne Taulukko 1. Potentiometrisen mittausmenetelmän valinta.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Etusivu > Analyysimenetelmät > 6.2. Potentiometria |
Edellinen | Seuraava | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
